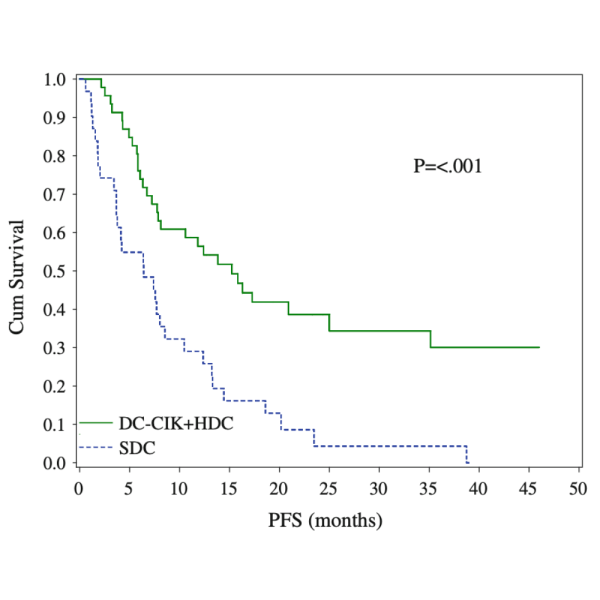
In dieser Studie untersuchten die Forscher die potenziellen Vorteile der Kombination von den Dendritischen Zellen (DZ) mit einer autologen Zytokin-induzierten Killer-(CIK)-Immuntherapie neben einer Hochdosis-Chemotherapie (HDC) für Patienten mit metastasiertem Brustkrebs (MBC). Die Ergebnisse der Studie zeigten, dass die Kombinationstherapie aus HDC und DC/CIK bei MBC-Patienten hochwirksam war. Insbesondere die Verwendung eines spezifischen HDC-Regimes in Verbindung mit einer DC/CIK-Immuntherapie zeigte vielversprechende klinische Vorteile im Vergleich zur alleinigen Chemotherapie. Diese Forschung unterstreicht das Potenzial der Kombination verschiedener Behandlungen, um Patienten einen umfassenderen und wirksameren Ansatz zur Krebsbehandlung zu bieten.
Die Wahl eines geeigneten Schemas einer Hochdosis-Chemotherapie in Kombination mit einer adoptiven Zelltherapie mit den Dendritischen und Zytokin-induzierten Killerzellen verbesserte das progressionsfreie Überleben und das Gesamtüberleben bei Patientinnen mit metastasiertem Brustkrebs: eine Neubegründung solch umstrittener therapeutischer Präferenzen.
Die Auswahl eines geeigneten Regimes einer hochdosierten Chemotherapie in Kombination mit einer adoptiven Zelltherapie mit den Dendritischen und Zytokin-induzierten Killerzellen verbesserte das progressionsfreie Überleben und das Gesamtüberleben bei Patientinnen mit Brustkrebs mit Span- und Pfund-Metastasen: eine Neubegründung solch umstrittener therapeutischer Präferenzen.
Unsere früheren Arbeiten haben gezeigt, dass Thiotepa Brustkrebsstammzellen ausrotten kann. Von 2004 bis 2009 erhielten 79 Patienten eine Standarddosis-Chemotherapie (SDC) mit 75 mg/m2 Docetaxel und 75 mg/m2 Thiotepa im Vergleich zu 87 Patienten mit HDC – DC/CIK: 120 mg/m2 Docetaxel zur Mobilisierung peripherer CD34? Vorläuferzellen, eine Sequenz von HDC (120 mg/m2 Docetaxel, plus 175 mg/m2 Thiotepa) – DC/CIK, mit oder
ohne 400 mg/m2 Carboplatin, abhängig von der Knochenmarksfunktion.
Die Endpunkte waren Ansprechraten (RR), progressionsfreies Überleben (PFS) und Gesamtüberleben (OS).
Ergebnisse Im Vergleich zu SDC waren PFS und OS bei HDC – DC/CIK verbessert (medianes PFS 10,2 vs. 3,7 Monate, P \ 0,001; medianes OS 33,1 vs. 15,2 Monate, P \ 0,001). Patienten mit prämenopausaler HDC als Erstlinienbehandlung nach Metastasierung oder mit viszeraler Metastasierung zeigten ein verlängertes PFS und OS. Auch die SDC-Gruppe erzielte eine ähnliche Resonanz wie frühere Berichte.
Obwohl diese Studie nicht als vollständige prospektive klinische Studie betrachtet werden konnte, wurden 166 Patienten in dieser Vergleichsstudie in HDC plus adoptive Zelltherapie mit DC/CIK-Zellen oder Chemotherapie in Standarddosis eingeteilt. Während die komplexe Natur unseres Behandlungsplans zusätzliche Studien erfordert, um die Rolle der einzelnen Komponenten, einschließlich autologem DC, CIK und hochdosiertem Docetaxel und Thiotepa, zu bestimmen, haben wir die Machbarkeit und Verträglichkeit eines kombinierten Therapieplans nachgewiesen Chemo plus Immuntherapie. Unseres Wissens nach könnte es die erste Studie sein, die alle Elemente in der Behandlung von Patienten vereint
mit MBC.
Diese Studie zeigte, dass die neuartige Kombination von HDC mit DC/CIK eine wirksame Wahl für die ausgewählte MBC-Population ist, bei der die Auswahl geeigneter Chemotherapien eine wichtige Rolle spielte und auch ein spezifisches HDC-Regime plus DC/CIK-Immuntherapie die klinischen Vorteile im Vergleich zeigte allein mit Chemotherapie.
Referenzlink zum Artikel: Klicken Sie hier
Veröffentlichungsdatum des wissenschaftlichen Artikels: 01.03.2013
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland
International
For Germany, Austria and Switzerland