En este estudio, se analizan los resultados de seguridad y supervivencia de pacientes con melanoma con enfermedad metastásica regional que se sometieron a una disección regional de ganglios linfáticos (RLND) y recibieron vacunación adyuvante con células dendríticas (DC). Al evaluar la seguridad y eficacia de este enfoque terapéutico, se espera ofrecer nuevas opciones terapéuticas a los pacientes con melanoma que se enfrentan a una enfermedad metastásica regional. El uso de la vacunación con CD como terapia adyuvante tras la RLND ha resultado prometedor en estudios preclínicos y puede ayudar a mejorar la inmunidad antitumoral en estos pacientes.
La incidencia del melanoma cutáneo sigue aumentando en todo el mundo. La resección quirúrgica adecuada sigue siendo el tratamiento estándar para los pacientes con enfermedad no sistémica. Sin embargo, aproximadamente el 15-20% de los pacientes con melanoma cutáneo desarrollarán metástasis regionales (ganglios linfáticos). Las DC, las células presentadoras de antígenos más eficaces del sistema inmunitario, se aprovechan para inducir células T citotóxicas específicas de melanoma en pacientes con melanoma. Las DC inmaduras son muy eficaces en la captación de antígenos y, cuando son estimuladas por mediadores inflamatorios y «señales de peligro», maduran y migran de los tejidos periféricos a los órganos linfoides.
Los pacientes se dividen en dos grupos.
Los pacientes con melanoma del grupo de inmunoterapia (n=78) recibieron adyuvante Vacuna de células dendríticas.
La vacunación DC consistió en un máximo de tres ciclos de tres vacunaciones quincenales. De todos los pacientes, 54 de 78 recibieron los tres ciclos completos de vacunación.
Vacunación con células dendríticas
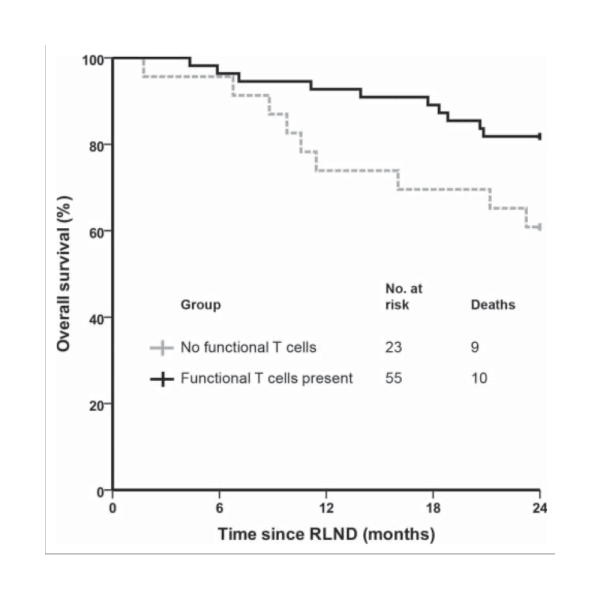
Se detectaron células T funcionales específicas de tumor en 55 de los 78 pacientes vacunados (71%).La tasa de supervivencia a los 2 años fue significativamente mayor (82%) en los pacientes con células T funcionales específicas de tumor en comparación con los pacientes vacunados con DC sin células T funcionales específicas de tumor 61% (p = 0,04).
Toxicidad
En general, las vacunas DC fueron bien toleradas. Cuarenta y ocho de 57 pacientes (84%) que recibieron sólo vacunas de CC y 20 de 21 pacientes (95%) que recibieron tanto vacunas de CC como IL-2 sufrieron al menos un acontecimiento adverso leve (CTC de grado 1 o 2).
Los efectos secundarios más frecuentes asociados a la vacunación con CD son síntomas gripales transitorios, como fatiga y fiebre, y eritema en el lugar de la inyección. No se observó toxicidad de grado 3 o 4 relacionada con el tratamiento. Se interrumpió el tratamiento en dos pacientes a petición propia debido a una erupción cutánea de grado dos relacionada con la vacuna en el segundo ciclo; ambos pacientes siguen vivos (94 y 115 meses después de la RLND).
Supervivencia
La mediana de la SG aumentó más del doble en los pacientes que recibieron la vacunación adyuvante con CD en comparación con el grupo de control, de 31,0 (IC del 95%: 23,6-38,5) a 63,6 meses (IC del 95%: 24,5-102,7) (p = 0,018). Para los pacientes que recibieron la vacuna DC (n=78), la tasa de SG a 1 año es del 87%, la tasa de SG a 2 años es del 76% y la tasa de supervivencia a 5 años es del 53% Y para el grupo Control (n=209), la tasa de SG a 1 año es del 74%, la tasa de SG a 2 años es del 59% y la tasa de SG a 5 años es del 38% (p = 0,018; p = 0,009; p = 0,008, respectivamente). En cuanto al tiempo transcurrido hasta la metástasis a distancia, se observó una tendencia a favor de los pacientes vacunados con CD, con una mediana de 41,9 meses (IC del 95%: 32,3-51,4) frente a 24,3 meses en el grupo de control (IC del 95%: 18,9-29,7; p = 0,081).
El tratamiento adyuvante con vacunación de DC después de RLND en pacientes con metástasis regional de melanoma es seguro y resulta en una SG favorable en comparación con los controles emparejados. Es importante destacar que CD
es bien tolerada y claramente menos tóxica que el IFN-α adyuvante o el ipilimumab. Estos resultados sugieren que la vacunación con DC tiene eficacia como tratamiento adyuvante del melanoma y proporcionan más apoyo para probarlo en un ensayo clínico prospectivo aleatorizado.
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland