In dieser Studie werden die Sicherheits- und Überlebensergebnisse von Melanompatienten mit regionaler Metastasierung analysiert, die sich einer regionalen Lymphknotendissektion (RLND) unterzogen und eine adjuvante Impfung gegen den Dendritische Zellen (DZ) erhalten haben. Durch die Bewertung der Sicherheit und Wirksamkeit dieses Behandlungsansatzes besteht die Hoffnung, neue Therapiemöglichkeiten für Melanompatienten mit regionaler Metastasierung bereitzustellen. Der Einsatz der DZ-Impfung als adjuvante Therapie nach RLND hat sich in präklinischen Studien als vielversprechend erwiesen und könnte dazu beitragen, die Antitumorimmunität dieser Patienten zu stärken.
Die Inzidenz kutaner Melanome nimmt weltweit weiter zu. Eine adäquate chirurgische Resektion bleibt der Standard der Versorgung von Patienten mit nicht systemischen Erkrankungen. Allerdings entwickeln etwa 15–20 % der Patienten mit kutanem Melanom regionale (Lymphknoten-)Metastasen. DZs, die wirksamsten Antigen-präsentierenden Zellen des Immunsystems, werden genutzt, um bei Melanompatienten melanomspezifische zytotoxische T-Zellen zu induzieren. Unreife DZs sind sehr effektiv bei der Antigenaufnahme und wenn sie durch Entzündungsmediatoren und „Gefahrensignale“ stimuliert werden, reifen sie heran und wandern von peripheren Geweben zu lymphatischen Organen.
Die Patienten werden in zwei Gruppen eingeteilt.
Die Patienten der Immuntherapiegruppe (n = 78) mit Melanom wurden mit einem unterstützenden Impfstoff für die Dendritische Zellen behandelt.
Die DZ-Impfung bestand aus maximal drei Zyklen mit drei zweiwöchentlichen Impfungen. Von allen Patienten erhielten 54 von 78 Patienten die gesamten drei Impfzyklen.
Impfung mit den Dendritischen Zellen
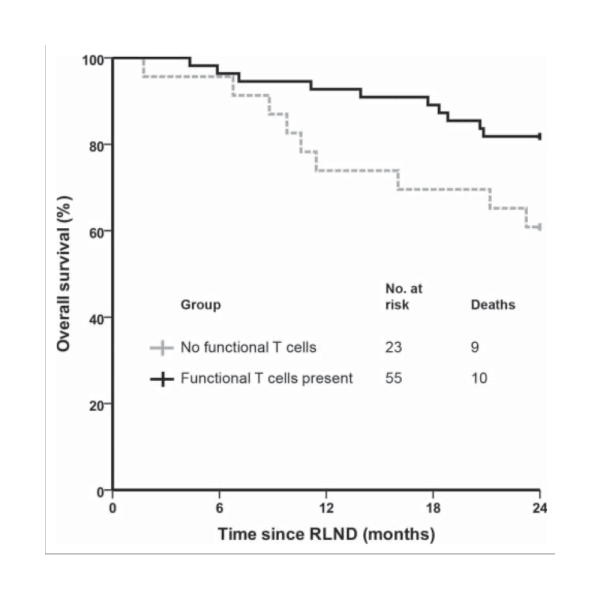
Funktionelle tumorspezifische T-Zellen wurden bei 55 von 78 geimpften Patienten (71 %) nachgewiesen. Die 2-Jahres-Überlebensrate war bei Patienten mit funktionellen tumorspezifischen T-Zellen signifikant höher (82 %) im Vergleich zu DZ-geimpften Patienten ohne funktionellen Tumor -spezifische T-Zellen 61 % (p = 0,04).
Schädliche Auswirkungen
DZ-Impfungen wurden im Allgemeinen gut vertragen. Achtundvierzig von 57 Patienten (84 %), die nur DZ-Impfungen erhielten, und 20 von 21 Patienten (95 %), die sowohl DZ-Impfungen als auch IL-2 erhielten, erlitten mindestens ein leichtes unerwünschtes Ereignis (CTC-Grad 1 oder 2).
Die häufigsten Nebenwirkungen, die mit der DZ-Impfung einhergehen, sind vorübergehende grippeähnliche Symptome, einschließlich Müdigkeit, Fieber und Erythem an der Injektionsstelle. Es wurde keine behandlungsbedingte Toxizität vom Grad 3 oder 4 beobachtet. Bei zwei Patienten wurde die Behandlung aufgrund eines impfbedingten Ausschlags zweiten Grades im zweiten Zyklus auf eigenen Wunsch abgebrochen, beide Patienten sind noch am Leben (94 und 115 Monate nach RLND).
Überleben
Das mittlere OS erhöhte sich bei Patienten, die eine adjuvante DZ-Impfung erhielten, im Vergleich zur Kontrollgruppe um mehr als das Doppelte, von 31,0 (95 %-KI 23,6–38,5) auf 63,6 Monate (95 %-KI 24,5–102,7) (p = 0,018). Bei Patienten, die eine DZ-Impfung erhielten (n = 78), beträgt die 1-Jahres-OS-Rate 87 %, die 2-Jahres-OS-Rate 76 % und die 5-Jahres-Überlebensrate 53 %. Für die Kontrollgruppe (n = 209) beträgt die 1 Die 1-Jahres-OS-Rate beträgt 74 %, die 2-Jahres-OS-Rate 59 % und die 5-Jahres-OS-Rate 38 % (p = 0,018; p = 0,009; p = 0,008). Bei der Zeit bis zur Fernmetastasierung zeigte sich ein Trend zugunsten der DZ-geimpften Patienten mit einem Median von 41,9 Monaten (95 %-KI 32,3–51,4) gegenüber 24,3 Monaten in der Kontrollgruppe (95 %-KI 18,9–29,7; p =). 0,081)
Die ergänzende Therapie mit DZ-Impfung nach RLND bei Patienten mit regionaler Melanommetastasierung ist sicher und führt im Vergleich zu entsprechenden Kontrollgruppen zu einer verbesserten Überlebensrate. Wichtig, DZ
Die Impfung ist gut verträglich und deutlich weniger toxisch als adjuvantes IFN-α oder Ipilimumab. Diese Ergebnisse deuten darauf hin, dass die DZ-Impfung als adjuvante Behandlung von Melanomen wirksam ist, und bieten weitere Unterstützung, um dies in einer prospektiven randomisierten klinischen Studie zu testen.
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland
International
For Germany, Austria and Switzerland