Cette étude analyse l’innocuité et les résultats en termes de survie de patients atteints de mélanome avec une maladie métastatique régionale qui ont subi une dissection régionale des ganglions lymphatiques (RLND) et ont reçu une vaccination adjuvante par cellules dendritiques (CD). En évaluant la sécurité et l’efficacité de cette approche thérapeutique, on espère offrir de nouvelles options thérapeutiques aux patients atteints de mélanome et confrontés à une maladie métastatique régionale. L’utilisation de la vaccination par CD comme thérapie adjuvante après la RLND s’est avérée prometteuse dans les études précliniques et pourrait contribuer à renforcer l’immunité anti-tumorale chez ces patients.
L’incidence du mélanome cutané continue d’augmenter dans le monde entier. Une résection chirurgicale adéquate reste la norme de soins pour les patients atteints d’une maladie non systémique. Cependant, environ 15 à 20 % des patients atteints de mélanome cutané développeront des métastases régionales (ganglions lymphatiques). Les CD, les cellules présentatrices d’antigènes les plus efficaces du système immunitaire, sont exploitées pour induire des cellules T cytotoxiques spécifiques du mélanome chez les patients atteints de mélanome. Les CD immatures sont très efficaces dans l’absorption d’antigènes et, lorsqu’elles sont stimulées par des médiateurs inflammatoires et des « signaux de danger », elles deviennent matures et migrent des tissus périphériques vers les organes lymphoïdes.
Les patients sont divisés en deux groupes.
Groupe d’immunothérapie (n=78) : les patients atteints de mélanome ont reçu un vaccin adjuvant à base de cellules dendritiques.
La vaccination par CD a consisté en un maximum de trois cycles de trois vaccinations bihebdomadaires. Sur l’ensemble des patients, 54 des 78 patients ont reçu les trois cycles complets de vaccination.
Vaccination par cellules dendritiques
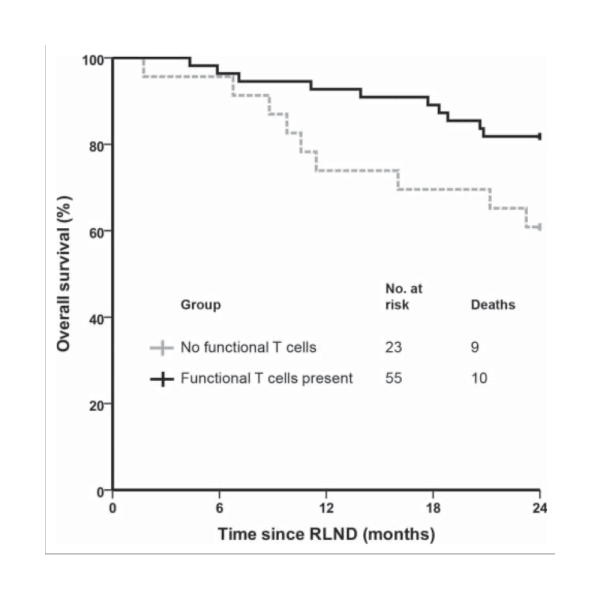
Le taux de survie à 2 ans était significativement plus élevé (82%) chez les patients ayant des cellules T fonctionnelles spécifiques de la tumeur que chez les patients vaccinés par CD sans cellules T fonctionnelles spécifiques de la tumeur (61%) (p = 0,04).
Toxicité
Les vaccinations par CD ont été généralement bien tolérées. Quarante-huit des 57 patients (84 %) ayant reçu uniquement des vaccins CD et 20 des 21 patients (95 %) ayant reçu à la fois des vaccins CD et de l’IL-2 ont souffert d’au moins un effet indésirable léger (grade CTC 1 ou 2).
Les effets secondaires les plus courants associés à la vaccination CD sont des symptômes transitoires de type grippal, notamment la fatigue et la fièvre, ainsi qu’un érythème au point d’injection. Aucune toxicité de grade 3 ou 4 liée au traitement n’a été observée. Le traitement a été interrompu chez deux patients à leur propre demande en raison d’une éruption cutanée de grade 2 liée au vaccin au cours du deuxième cycle ; les deux patients sont toujours en vie (94 et 115 mois après la RLND).
Survie
La durée médiane de survie a été multipliée par plus de deux chez les patients ayant reçu une vaccination adjuvante par CD par rapport au groupe témoin, passant de 31,0 (IC 95 % 23,6-38,5) à 63,6 mois (IC 95 % 24,5-102,7) (p = 0,018). Pour les patients ayant reçu la vaccination CD (n=78), le taux de survie à 1 an est de 87%, le taux de survie à 2 ans est de 76% et le taux de survie à 5 ans est de 53%. Pour le groupe de contrôle (n=209), le taux de survie à 1 an est de 74%, le taux de survie à 2 ans est de 59% et le taux de survie à 5 ans est de 38% (p = 0,018 ; p = 0,009 ; p = 0,008, respectivement). En ce qui concerne le temps écoulé jusqu’à la métastase à distance, une tendance a été observée en faveur des patients vaccinés par CD, avec une médiane de 41,9 mois (IC à 95 % 32,3-51,4) contre 24,3 mois dans le groupe témoin (IC à 95 % 18,9- 29,7 ; p = 0,081).
Le traitement adjuvant par vaccination CD après RLND chez les patients atteints de métastases régionales de mélanome est sûr et permet d’obtenir une SG favorable par rapport à des contrôles appariés. Il est important de noter que la vaccination par CD
est bien tolérée et nettement moins toxique que l’IFN-α adjuvant ou l’ipilimumab. Ces résultats suggèrent que la vaccination par CD est efficace en tant que traitement adjuvant du mélanome et apportent un soutien supplémentaire à la réalisation d’un essai clinique prospectif randomisé.
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland