In diesem innovativen Forschungsprojekt erhalten Patienten mit Lungenkrebs eine personalisierte Behandlung mit einem autologen DZ-Impfstoff, der mit spezifischen Neoantigen-Peptiden angereichert ist. Dieser Ansatz markiert einen vielversprechenden Durchbruch im Bereich der Therapie von Lungenkrebs. Die gezielte Abwehr von Neoantigenen hat beträchtliches Potenzial zur Anregung der natürlichen Immunreaktion des Körpers gegenüber Krebszellen aufgezeigt. Der personalisierte Charakter des Impfstoffs ermöglicht maßgeschneiderte Behandlungspläne, die individuelle Patientenmerkmale berücksichtigen und letztendlich zu besseren Ergebnissen und einer besseren Lebensqualität führen.
Patienten mit histologisch oder zytologisch bestätigtem Lungenkrebs, einschließlich Plattenepithelkarzinom, Adenokarzinom, neuroendokrinem Tumor und SCLC, im Alter zwischen 18 und 75 Jahren mit mindestens einer messbaren Krankheit gemäß RECIST. Der Patient muss sich Standardtherapien unterzogen haben und seine Krankheit ist fortgeschritten. Die Lebenserwartung sollte mindestens 3 Monate betragen. Leistungsstatus der Eastern Cooperative Oncology Group (ECOG) von 0 oder 1 sowie ausreichende Knochenmarks-, Nieren- und Leberfunktionen.
DNA- und RNA-Präparation
Tumorgewebe wurden durch Faserbronchoskopiebiopsie, supraklavikuläre metastatische Lymphknotenresektion, Feinnadelaspiration metastatischer Lendenläsionen und Feinnadelaspiration von Lungentumorläsionen gewonnen und später mit 1 ml RNA gelagert (Thermo Fisher, Nr. AM7020). Es wurde Blut gesammelt und mit einem EDTA-basierten Antikoagulans vermischt. DNA und RNA wurden mit dem All Prep DNA/RNA Mini Kit aus demselben Tumorgewebe extrahiert, und DNA aus EDTA-antikoaguliertem peripherem Blut wurde mit dem QIAamp DNA Blood Mini Kit extrahiert. Die Qualität der DNA/RNA wurde mit dem 2100 Bioanalyzer bewertet. Für den anschließenden Sequenzierungsprozess wurden für jeden Patienten Trioproben (zwei DNA-Proben aus Tumor und Blut und eine RNA-Probe nur aus dem Tumor) vorbereitet.
Extraktion von DNA und RNA
Tumorgewebe wurden durch Faserbronchoskopiebiopsie, supraklavikuläre metastatische Lymphknotenresektion, Feinnadelaspiration metastatischer Lendenläsionen und Feinnadelaspiration von Lungentumorläsionen gewonnen und später mit 1 ml RNA gelagert (Thermo Fisher, Nr. AM7020). Es wurde Blut gesammelt und mit einem EDTA-basierten Antikoagulans vermischt. DNA und RNA wurden mit dem All Prep DNA/RNA Mini Kit aus demselben Tumorgewebe extrahiert, und DNA aus EDTA-antikoaguliertem peripherem Blut wurde mit dem QIAamp DNA Blood Mini Kit extrahiert. Die Qualität der DNA/RNA wurde mit dem 2100 Bioanalyzer bewertet. Für den anschließenden Sequenzierungsprozess wurden für jeden Patienten Trioproben (zwei DNA-Proben aus Tumor und Blut und eine RNA-Probe nur aus dem Tumor) vorbereitet.
PBMCs wurden aus dem peripheren Blut der Patienten isoliert. 5–10 × 106/ml ausgewaschene PBMCs wurden in T175-Kolben mit AIM-V-Medium inokuliert und 3 Stunden lang bei 37 °C und 5 % CO2 inkubiert. Anschließend wurden die suspendierten Zellen gesammelt und in flüssigem Stickstoff eingefroren. Die anhaftenden Zellen wurden gewaschen und in AIM-V-Medium kultiviert, das 1 % autologes Serum, humanes GM-CSF klinischer Qualität (1000 IU/ml) und tierversuchsfreies IL-4 in Forschungsqualität (500 IU/ml) enthielt. Nach 5 Tagen wurden die Neoantigen-Peptide (50 μg/ml) zu den unreifen DZs gegeben. Nach 20–24 Stunden Peptidbeladung wurden die DZs mit TNF-α (10 ng/ml), IL-1β (10 ng/m), IFN-γ (1000 U/ml) und Prostaglandin E2 (PGE2, 250 ng/ml) gereift ) R848 (1 μg/ml) und Polyinosin-Polycytidylsäure (20 ng/ml; Poly (I:C)) gemischt und 20–24 Stunden lang inkubiert.
Die Patienten wurden einen Tag vor der Injektion von Neo-DCVac mit Cyclophosphamid in einer Dosis von 250 mg/m2 vorbehandelt. Das vorbereitete Neo-DCVac wurde am Tag 0 beidseitig subkutan in die Achsel- und Leistengegend geimpft. GM-CSF wurde in den folgenden 5 Tagen (Tage 1–5) in einer Dosis von 0,075 mg verabreicht.
Nebenwirkungen und Toxizität
Alle unerwünschten Ereignisse waren auf Grad 1 oder 2 beschränkt. Bei allen Patienten traten Hautreaktionen des Grades 1 an der Injektionsstelle auf. Patient 4 entwickelte nach der Behandlung mit Neo-DCVac eine vorübergehende Neutropenie Grad 1, die ohne Behandlung gelindert wurde. Patient 12 entwickelte einen juckenden Ausschlag Grad 2 am gesamten Rumpf und an den Extremitäten. Es wurde keine andere spezifische Behandlung verabreicht und sein Ausschlag ließ nach, nachdem die Impfung beendet wurde. Neo-DCVac erhöhte das Risiko immunbedingter unerwünschter Ereignisse im Zusammenhang mit ICIs nicht. Keine Toxizität war dosislimitierend oder führte zu einer Dosisverzögerung oder einem Abbruch der Behandlung.
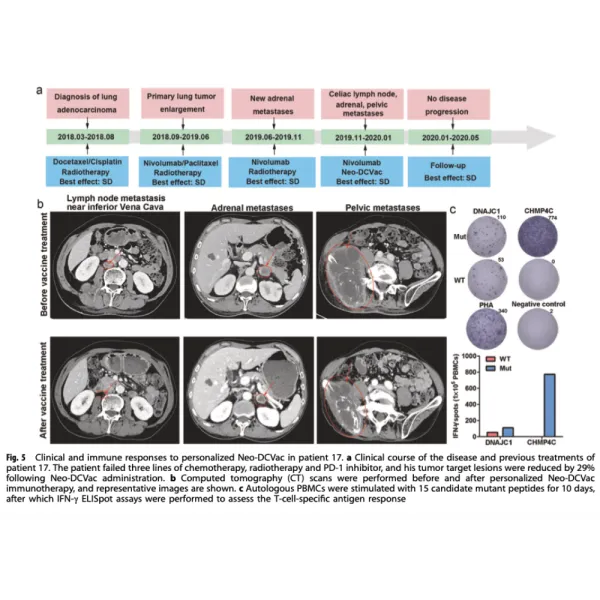
Das mittlere progressionsfreie Überleben (PFS) betrug 5,5 Monate (95 %-Konfidenzintervall (KI: 1,9–9,2)) und das mittlere Gesamtüberleben (OS) betrug 7,9 Monate (95 %-KI: 5,9–10,0). Drei (25 %) der 12 Patienten erreichten ein objektives Ansprechen. Bei allen Antworten handelte es sich um PR, es wurden keine vollständigen Antworten (CRs) aufgezeichnet. Bei sechs (50 %) von 12 Patienten kam es zu einer Verringerung der Größe ihrer Zielläsionen, neun (75 %) von 12 Patienten erreichten eine Krankheitskontrolle und bei drei Patienten (25 %) wurde eine fortschreitende Erkrankung (PD) verzeichnet.
Die Ergebnisse dieser Pilotstudie haben bewiesen, dass Neo-DCVac machbar, sicher und in der Lage ist, eine spezifische T-Zell-Immunität und einen therapeutischen Nutzen hervorzurufen. Die ersten Erkenntnisse zur Aktivität einer Neoantigen-basierten DZ-Impfstoffbehandlung bei Patienten mit fortgeschrittenem NSCLC. Von größter Bedeutung ist vielleicht, dass Neo-DCVac Auswirkungen auf eine Vielzahl von Krebsarten haben könnte.
Referenzlink zum Artikel: Klicken Sie hier
Veröffentlichungsdatum des wissenschaftlichen Artikels 21.01.2021
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland
International
For Germany, Austria and Switzerland