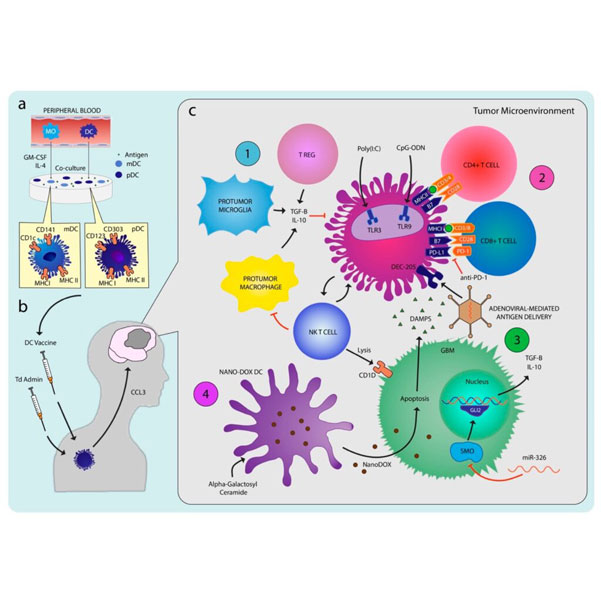
Le glioblastome (GBM) est une tumeur maligne primaire du système nerveux central dévastatrice chez les adultes, avec des options de traitement limitées et un taux de survie moyen de moins de 15 mois. Si la chirurgie, la radiothérapie et la chimiothérapie sont les traitements standard, ils n’offrent que des avantages modestes et les récidives sont fréquentes. Compte tenu du mauvais pronostic du GBM, il est urgent de mettre au point de nouvelles thérapies. L’immunothérapie utilisant les cellules dendritiques (CD) est apparue comme une approche prometteuse pour renforcer la réponse immunitaire anti-tumorale de l’organisme. En tant que cellules présentatrices d’antigènes « professionnelles », les CD jouent un rôle crucial dans l’initiation des réponses immunitaires contre les tumeurs. Des études précliniques ont démontré une survie prolongée et une mémoire immunitaire dans des modèles murins de GBM grâce à la stimulation de l’activité des CD à l’aide de divers antigènes et molécules de costimulation.
De Vleesvchouwer et al. et Wheeler et al. ont mené de vastes essais de phase II avec 56 patients atteints de GBM et 23 patients atteints de GBM, respectivement. Dans l’étude de De Vleesvchouwer, des patients >âgés de 3 ans ont été enrôlés dans un essai prospectif de comparaison de cohortes (HGG-IMMUNO) dans lequel des patients atteints de GBM récurrent ont été traités avec des DCV pulsés avec des cellules tumorales autologues dans trois cohortes, où chaque cohorte a servi de contrôle historique pour les cohortes suivantes. Dans la cohorte A, le DCV a été administré à la semaine 1 et à la semaine 3, puis toutes les 4 semaines. Dans la cohorte B, cinq vaccins CD ont été administrés à des intervalles de 2 semaines, puis toutes les 4 semaines. Dans la cohorte C, 4 vaccinations hebdomadaires par CD ont été effectuées avec des injections intradermiques de lysat tumoral en guise de rappel. Les auteurs ont constaté une tendance à l’amélioration de la SSP et de la SG chez les patients âgés de moins de 35 ans. Une analyse de sous-groupes de patients âgés de plus de 21 ans a montré une amélioration de la SSP et de la SG dans la cohorte C, c’est-à-dire chez les patients traités par des administrations hebdomadaires de vaccins et des rappels. Wheeler et al. ont étudié l’efficacité du DCV pulsé par lysat tumoral administré par voie sous-cutanée à 33 patients atteints de GBM, 23 récurrents et 11 nouvellement diagnostiqués, à des intervalles de 2 semaines pour trois doses et une quatrième vaccination 6 semaines après la troisième. Un patient a développé un GBM métastatique autour du site d’injection du vaccin. On pense que cela est dû à la croissance de rares cellules tumorales résistantes aux radiations présentes chez ce patient particulier et non à des métastases de la tumeur primaire d’origine. La SSP et la SG des personnes vaccinées se comparent favorablement à celles des patients qui n’ont pas reçu de traitement par DCV dans l’institution où s’est déroulé l’essai pendant la durée de celui-ci. Dix-sept des 34 patients atteints de GBM ont présenté une réponse vaccinale positive, sept d’entre eux présentant >une production d’IFN-γ multipliée par 1,5 avant la vaccination, ce qui suggère une réponse anti-tumorale endogène. Ils ont constaté que la survie médiane chez les personnes ayant répondu au vaccin était de 642 jours, contre 430 jours chez les personnes n’ayant pas répondu au vaccin. La PFS était de 308 jours chez les répondeurs au vaccin, contre 167 jours chez les non-répondeurs.
Des études précliniques et cliniques ont démontré une réponse immunologique mesurable et des taux de survie plus ou moins prolongés. Diverses combinaisons d’adjuvants synergiques visant à surmonter les diverses immunosuppressions induites par le gliome se sont révélées prometteuses. Le rapport intermédiaire du premier essai de phase III du DCV dans les GBM nouvellement diagnostiqués confirme la sécurité et la faisabilité et suggère une survie plus longue que prévu avec le DCV. Alors que nous attendons avec impatience les résultats finaux de l’étude et les résultats d’autres études de phase III, il est nécessaire d’explorer davantage la combinaison optimale de thérapies immunitaires, l’intégration idéale de ces thérapies dans la norme actuelle de soins, et les phénotypes de répondeurs afin d’identifier les patients qui sont les plus susceptibles de bénéficier de la thérapie.
REGISTERED ADDRESS:
Immunyo Ltd
Kincora Ave 35
Clontarf
Dublin 3
Ireland
International
For Germany, Austria and Switzerland